#Notícias
#Notícias
Para diminuir custos e aumentar diversidade em estudos clínicos
Agência reguladora norte-americana sugere analisar eficácia de tratamentos unindo estudos observacionais com coletas de dados específicas
 De acordo com artigo publicado na revista científica JAMA, estudos clínicos pragmáticos têm "desenhos simplificados, prospectivos, ajustados para responder a uma questão específica, focada, e por vezes pode aplicar randomização, apesar de outros desenhos poderem ser usados” | Imagem: Shutterstock
De acordo com artigo publicado na revista científica JAMA, estudos clínicos pragmáticos têm "desenhos simplificados, prospectivos, ajustados para responder a uma questão específica, focada, e por vezes pode aplicar randomização, apesar de outros desenhos poderem ser usados” | Imagem: Shutterstock
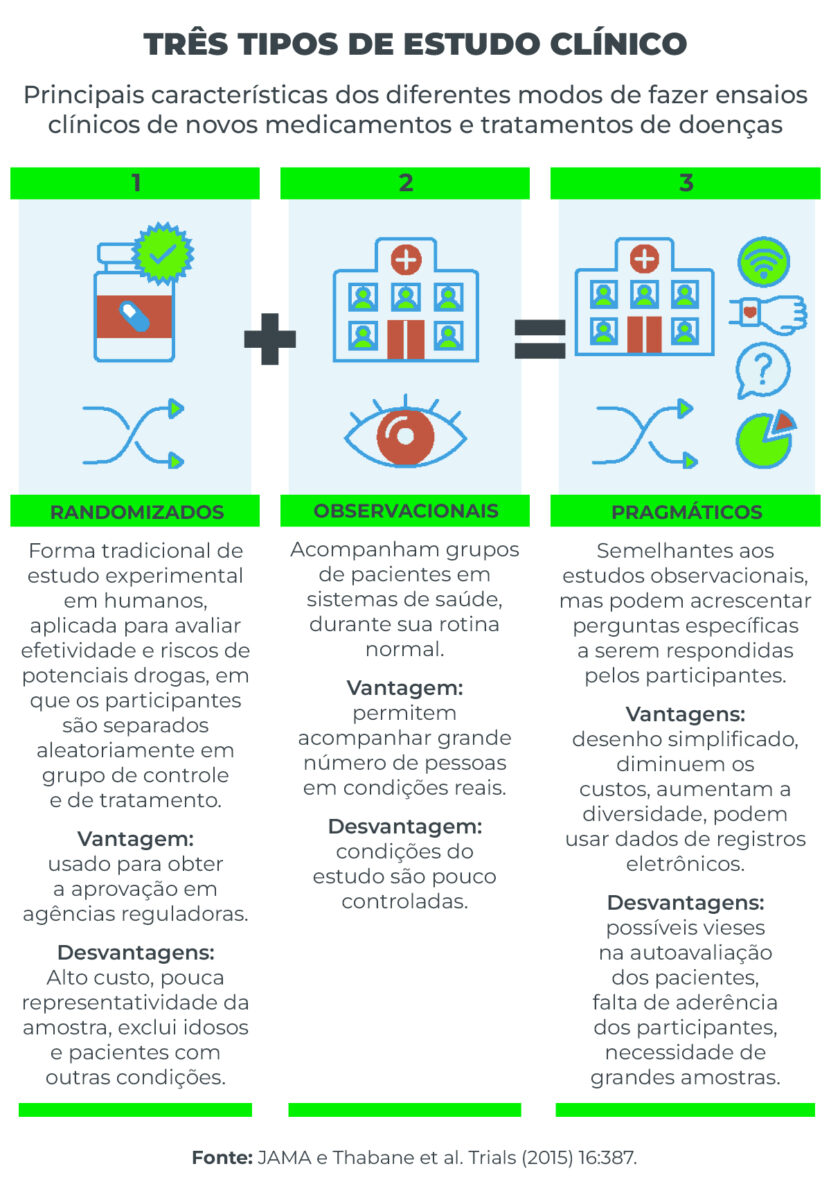
Os estudos clínicos randomizados são aqueles necessários para a aprovação de novos medicamentos e tratamentos por agências reguladoras, como a Agência Nacional de Vigilância Sanitária (Anvisa) no Brasil e a Food and Drug Admnistration (FDA) nos Estados Unidos.
Bastante complexos, tais estudos são custosos, o que às vezes inviabiliza sua execução.
Já os chamados estudos observacionais acompanham pacientes que fazem determinados tratamentos, a fim de avaliar alguma condição de saúde e os efeitos dos medicamentos usados.
Embora não desempenhem tanto controle das condições, os estudos observacionais têm como vantagem o uso de dados da vida real, incluindo um número maior de pacientes, o que pode proporcionar a detecção de efeitos adversos de magnitude elevada, mas pouco frequentes.
Em artigo publicado no periódico JAMA, da Associação Americana de Medicina, profissionais da FDA defendem um meio termo entre esses dois tipos de testes: os estudos clínicos pragmáticos.
De acordo com os autores, essa área de pesquisa merece mais atenção e ênfase.
“[Este tipo de estudo clínico] apresenta desenhos simplificados, prospectivos, ajustados para responder a uma questão específica, focada, e por vezes pode aplicar randomização, apesar de outros desenhos poderem ser usados”, escreveram Ali Abbasi, Lesley Curtis e Robert Califf.
Para os autores, um sistema de geração de evidências integrado à rotina de tratamento após a aprovação inicial dos medicamentos pode ser bastante promissor para avaliar riscos e benefícios, algo nem sempre totalmente contemplado no sistema de avaliação atual.
Custos altos e baixa diversidade
Os autores do artigo informam que este tipo de pesquisa é bastante promissor quando incorporado aos sistemas de saúde, podendo ajudar os pesquisadores a evitar problemas típicos dos estudos clínicos tradicionais.
Um deles, o alto custo, por vezes proibitivo, assim como a baixa diversidade, que pode ocorrer quando os testes clínicos são conduzidos em centros não representativos de todas as configurações e populações de pacientes.
Clique aqui para saber mais sobre o esforço de pesquisadores para tornar estudos clínicos mais diversos e representativos
Um sistema de geração de evidências integrado à rotina de tratamento após a aprovação inicial dos medicamentos é bastante promissor, diz o paper, para avaliar riscos e benefícios, algo nem sempre contemplado no sistema de avaliação atual.
Isso é particularmente verdadeiro em muitas áreas terapêuticas, mas especialmente para doenças crônicas comuns, como condições cardiovasculares, pulmonares, renais, diabetes tipo 2 e Alzheimer.
Nesses casos, completam, extensos estudos clínicos são necessários, uma vez que os efeitos dos tratamentos são por vezes modestos, enquanto os riscos e benefícios são distribuídos de forma heterogênea entre as populações afetadas.
De acordo com o artigo, a agência norte-americana FDA tem interesse em pesquisa clínica pragmática após a aprovação inicial do tratamento em várias áreas importantes.
“Há uma necessidade de dados robustos para informar a prática clínica, particularmente estudos confirmatórios pós-mercado”, ressaltam os autores.
“Estes testes podem se assemelhar mais às condições da prática do mundo real do que os estudos clínicos tradicionais. Podem, ainda, aproveitar desenhos mais pragmáticos para focar em elementos-chaves necessários para confirmar benefícios e riscos para as populações pretendidas”, escrevem.
Para recrutar uma amostra ampla e diversa de pacientes com baixo custo, além do desenho simplificado dos estudos, os autores sugerem utilizar como fontes de dados registros eletrônicos de saúde, sensores vestíveis – que coletam dados de saúde de quem os usa – e métodos virtuais incorporados à prática clínica.
*
É permitida a republicação das reportagens e artigos em meios digitais de acordo com a licença Creative Commons CC-BY-NC-ND.
O texto não deve ser editado e a autoria deve ser atribuída, incluindo a fonte (Science Arena).